هيئة الدواء: ضبط وتحريز تشغيلات سرنجة تحت الجلد مغشوشة بالسوق| مستند
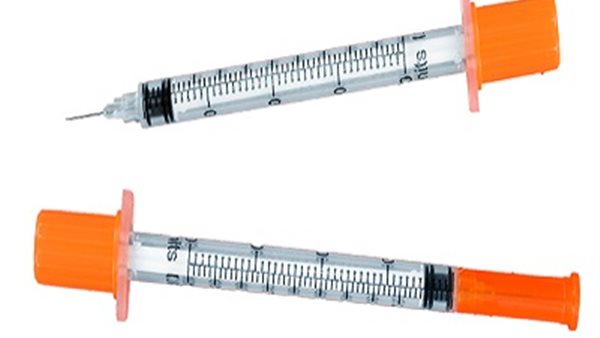
قررت الإدارة المركزية للعمليات، التابعة لهيئة الدواء المصرية، ضبط وتحريز كل العبوات من سرنجات إيكو سيرينج معقم تحت الجلد، تصنيع الدولية للمستلزمات الطبية.
ضبط وتحريز تشغيلات سرنجة تحت الجلد مغشوشة
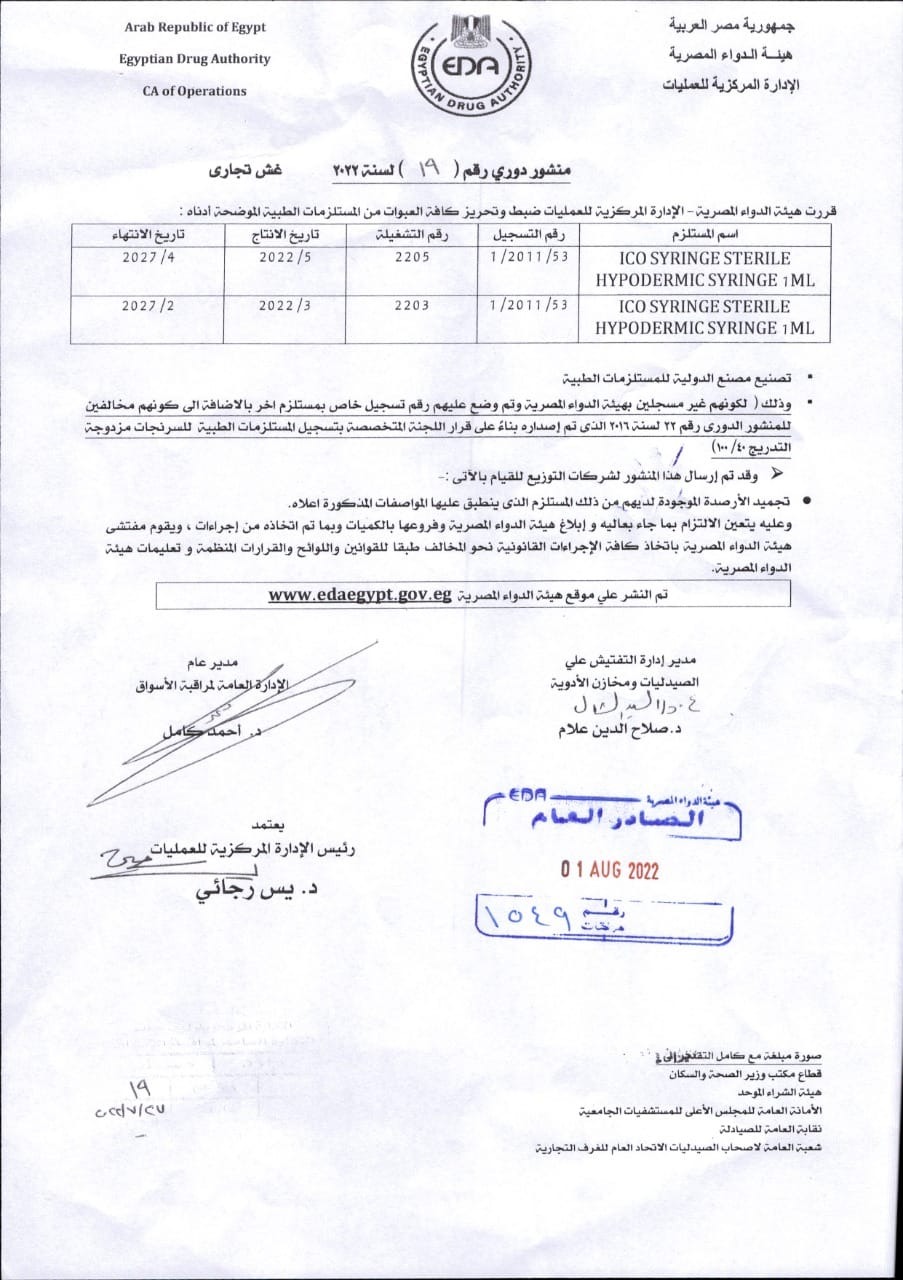
وأوضحت هيئة الدواء المصرية، في منشور لها، حصل القاهرة 24 على نسخة منه، أنه تقرر ضبط وتحريز تشغيلات من ICO SYRINGE STERILE HYPODERMIC SYRINGE 1ML - سرنجات إيكو سيرينج معقم تحت الجلد، والتي تحمل رقم 2205، و2203، ورقم تسجيل 1/2011/53.
وأضافت هيئة الدواء المصرية، أن تلك التشغيلات من هذه الحقن، غير مسجلة، وتم وضع عليها رقم تسجيل خاص بمستلزم آخر، بالإضافة إلى كونها مخالفة للمنشور الدوري رقم 22 لسنة 2016، الذي تم إصداره بناء على قرار اللجنة المتخصصة بتسجيل المستلزمات الطبية للسرنجات مزدوجة.
وشددت هيئة الدواء المصرية، على تجميد الأرصدة الموجودة لديهم من ذلك المستلزم، الذي ينطبق عليه المواصفات المذكورة، واتخاذ مفتشي هيئة الدواء المصرية كل الإجراءات القانونية نحو المخالف.
وفي وقت سابق، قررت اللجنة الفنية لمراقبة الأدوية بهيئة الدواء المصرية، في جلستها بتاريخ 28 يوليو الماضي، عدم الموافقة على استقبال مستحضرات جديدة تحتوى على Gemifloxacin جميفلوكساسين، وهي مادة مضاد حيوي واسع الطيف، قاتلة للبكتريا، في أشكال الجرعات الفموية.
وقررت اللجنة الفنية كذلك، وقف إنتاج المستحضرات المسجلة، وإعطاء مهلة 3 أشهر من تاريخ انعقاد اللجنة؛ لتحاول توفيق الأوضاع، مشددة على رفع توصية لرئيس هيئة الدواء السحب المستحضرات من السوق وإلغاء تسجيل المستحضرات المسجلة بعد انتهاء هذه المهلة.
وأوضحت اللجنة أن مرجعيتها في القرار؛ بناء على قرار اللجنة العلمية المتخصصة المجمعة لأمراض الصدر، برفض تسجيل المستحضر، حيث أنه توجد بدائل من Quinolonen كينولونين، وهي مجموعة من المضادات الحيوية واسعة الطيف، أكثر أمانا في السوق المصري.
وأشارت اللجنة العلمية إلى أن التجربة العلمية عند استخدام المستحضر، أثبتت أنه يسبب طفحًا جلديًّا شديدًا، مضيفة أن ميزان المنافع للمخاطر، ليس في صالح المستحضر، وذلك طبقا لتقرير وكالة الأدوية الأوروبية - EMA.



















